アルツハイマー病の原因物質を「光触媒」で凝集、除去 東京大学研究グループが新治療法の可能性を発表
東京大学の研究グループが、近赤外線を照射することでアルツハイマー病の原因物質とされるタンパク質「アミロイドベータ」を効率的に集め、除去する作用をもつ人工的な光触媒を開発、モデルマウスとヒトのサンプルで実際に作用することを確認したと発表した。未だ根治療法のないアルツハイマー病に対する治療法となりうるとしているほか、他の神経変性疾患、アミロイド蓄積が要因とされる疾患にも有用である可能性があるとしている。
独自に「病原性のアミロイドベータだけに反応する光触媒」を開発
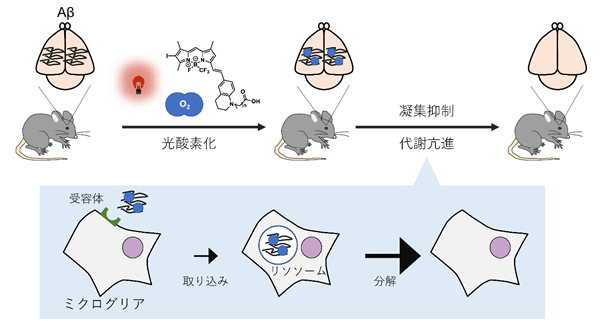
アルツハイマー病は脳内でのアミロイドβペプチド(Aβ)の凝集・蓄積が発症の原因とされることから、Aβの凝集を抑制すること、また凝集したAβを効率よく除去することが治療戦略として考えられているが、未だこれを実現する技術、療法ともに確立されていない。この課題に対し、東京大学大学院薬学系研究科機能病態学教室の富田泰輔教授、堀由起子講師、小澤柊太大学院生らと、同大学大学院有機合成化学教室の金井求教授、相馬洋平医薬機能グループリーダー(研究当時)らの研究グループは、近赤外線照射によって活性化する光触媒を用い、人為的に凝集したAβに選択的に酸素を付加する光酸素化法を開発した※1。
モデルマウスを用い、生きたマウス脳内でその作用を評価したところ、Aβのさらなる凝集を抑制し、かつ凝集Aβを脳内から効率的に除去できることが分かった。さらに光酸素化した凝集Aβの除去においては、脳内での免疫担当細胞であるミクログリア※2が関与し、ミクログリア細胞内のリソソーム分解酵素※3による分解が亢進していることも明らかになった。アルツハイマー病患者の死後脳サンプルでも同様の作用が確かめられたという。また同じくこの疾患の原因物質とされるタウアミロイドにおいても、同様に凝集を抑制し除去する作用も確かめられた。
研究グループではこれらの結果から、この技術がアルツハイマー病に対する有用な戦略となりうるとしているほか、開発した光触媒自体はアミロイドに共通の立体構造に対し反応するため、パーキンソン病や筋萎縮性側索硬化症などの神経変性疾患、さらには末梢にアミロイドが蓄積する様々な末梢性アミロイドーシスなどの疾患にも有用である可能性が期待できるとしている。この研究成果は査読付きの神経科学誌「Brain」に4月14日付で公開された。
※1 関連論文
研究グループは以前、この光触媒開発に関し2つの論文を発表している。
Switchable photooxygenation catalysts that sense higher-order amyloid structures(Nature Chemistry)
Near-Infrared Photoactivatable Oxygenation Catalysts of Amyloid Peptide(Chem)
※2 ミクログリア
脳内細胞の一つで、免疫反応を担当していると言われている。Abを取り込み、分解することが知られている。
※3 リソソーム分解酵素
細胞内小器官の一つであるリソソームに存在する分解酵素。リソソームは多くの分解酵素を有しており、タンパク質を分解していることが知られている。





